知道你的大脑:阿尔茨海默病
/背景
Auguste Deter,Alois Alzheimer的主题的案例研究描述了将被称为阿尔茨海默病的疾病。
1906年,在德国召开的一次精神病学家会议上,阿耳茨海默做了一次演讲,详细介绍了奥古斯特·德迪勒的不寻常案例。阿兹海默大约是在5年前遇到迪特的,当时他在德国梅因河畔法兰克福的一家精神病院担任助理医师。迪特在老年痴呆症上留下了深刻的印象,因为她相对年轻,但她患有一种独特的严重的,痴呆如症状。
当阿尔茨海默尔遇见她时,禁止51岁。当她的行为变得令人惊讶时,她最明显的症状已经开始。首先,她开始展现出丈夫的不具巧之声嫉妒。然后,她的记忆开始迅速恶化。她很容易变得迷失方向,并且经常与现实失去触感,偏执妄想消耗。正如老年痴呆症所描述的:
“...有时候她想有人试图杀死她,然后迎接像公司一样迎接主治医生......有时候她大声抗议,他打算削减她......然后她又是完全社会,绕着她的床上用品,呼叫拖累她的丈夫和女儿似乎遭受了幻觉。她经常尖叫好几个小时。“
阿尔茨海默氏症涉及案件。导致似乎受到一种老年精神病的折磨,这可能是痴呆症的症状。但很少见到痴呆症这是如此年轻的那么严重。
除了是一名医生,阿尔茨海默还是一名勤奋的研究人员。他对伴随精神和神经疾病的神经系统的病理变化非常感兴趣。因此,当迪特在55岁去世时,阿尔茨海默要求将她的大脑送到他那里进行研究。在检查中,阿尔茨海默氏症发现大脑遭受了广泛的神经元损失,并且充满了异常的结构(后来得知是下面讨论的蛋白质沉积)。
迪丝特的年龄,症状和神经退化让阿尔茨海默症认定她是个特例。在他的演讲中,在场的精神科医生似乎没有同样的感觉,然而,因为在他的演讲之后没有任何问题、评论或其他感兴趣的迹象(与会者似乎对下一次关于强迫性手淫的报告更感兴趣).但阿尔茨海默很少知道,他的演讲将标志着一个历史性的时刻,因为仅仅几年之后,著名的精神病学家(阿尔茨海默的同事)埃米尔·克雷佩林(Emil Kraepelin)引入了这个术语阿尔茨海默氏病描述一种早发的老年性痴呆。
直到20世纪70年代后期直到才研究人员开始认识到,大多数广告案件不是早期发作并发生在65岁以上的患者中。今天,广告是该年龄集团人民的最大健康问题之一,并且由于该人群的数量持续增加(讽刺地是,因此我们提高了让人们活着更长时间的能力,这是一个迅速增长的问题。今天,每隔10人在65岁以上约1人遭受广告以及美国患AD的人数预计到2050年将增长近两倍.
阿尔茨海默病的症状是什么?
广告是一种类型痴呆,这个术语用来描述涉及记忆丧失和其他认知困难的情况。痴呆症有许多不同的类型,然而,每一种都有自己的原因和特定的症状。AD只是一个变体。
阿尔茨海默病智力下降最明显的迹象是记忆问题。在疾病的早期阶段,这通常表现为创造新记忆的困难,问题尤其明显宣言回忆或者关于信息和事件的记忆(而不是如何进行如何进行常规事物,如绑鞋或与用具一起吃的东西,这被称为非陈述回忆).早期,患者通常能够保持较老的记忆和非陈述回忆。然而,随着时间的推移,所有内存都可能受到影响,即使是最持久的存储器也可能会恶化。
但内存缺陷只是广告症状学的一个方面。患者还可以遇到沟通问题,并且可能会损害阅读和写入的能力。可能发生不可预测的情绪骚乱,从冷漠和抑郁症到愤怒的爆发。思考经常变得妄想,而且相当一部分患者(高达20%)甚至会出现视觉幻觉.
然而,这不仅仅是受到影响的认知。运动受到阻碍,导致患者开始失去移动性,并且甚至在最简单的自我护理行为中表现出困难。咀嚼和吞咽等基本电机功能发生故障,并且最终发生失禁。
最后(如果病人活了这么长时间),没有多少大脑功能没有受到某种程度的影响,病人就会完全依赖护理人员的帮助,即使是最基本的日常活动,比如吃饭和上厕所。这种病总是致命的。
阿尔茨海默病的大脑发生了什么?
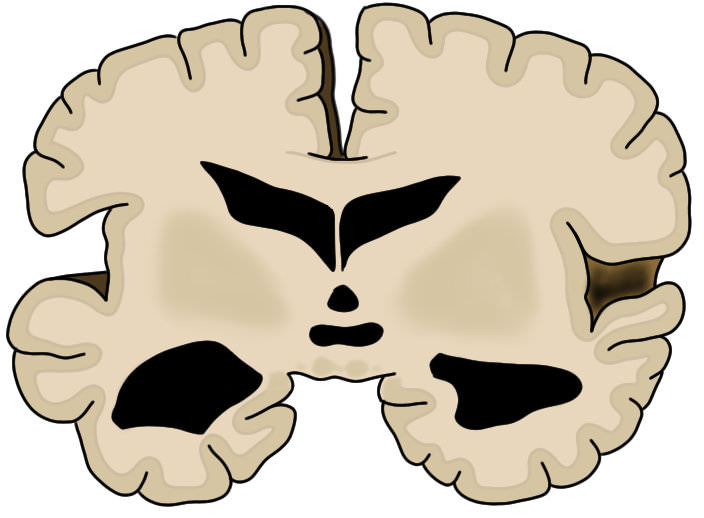
当Alois阿尔茨海默检查Auguste Deter的大脑时,他注意到一些明显的病理变化。第一种是大脑经历了严重的萎缩。与健康的大脑相比,它似乎有些萎缩。
这种AD脑的萎缩是由于在疾病中发生的脑细胞死亡。广告是所谓的神经退行性疾病,这是用于指导致神经元变性和死亡的疾病的分类。许多疾病属于这一类别(例如帕金森病,肌营养的外侧硬化),但广告是本集团最常见的疾病。
阿尔茨海默还注意到神经元内部和周围的异常形成。他说“分布在整个皮层……有……由一种特殊物质沉积而引起的病灶”,他还提到“许多纤维彼此相邻……它们一个接一个地出现在细胞表面。”阿尔茨海默氏症描述了AD的两个标志性神经症状淀粉样蛋白斑块和神经原纤维缠结.
第一种结构是淀粉样斑块,由小的肽(本质上是一种更小的蛋白质)β淀粉样蛋白或者,在神经元外形成大簇的Aβ。通常,酶称为蛋白酶可以帮助摆脱大脑中的不需要的肽和蛋白质。但淀粉样蛋白斑块尤其抵抗蛋白酶降解。因此,随着疾病的进展,它们在大脑中积聚;他们的存在是广告大脑的定义特征。
观看这段2分钟的神经科学视频,以摘要阿尔茨海默病的疾病影响大脑。
Alzheimer,神经纤维缠结的其他结构也由蛋白质的异常沉积组成。在这种情况下,称为蛋白质罪魁祸首TAU.Tau蛋白通常在帮助细胞运输物质方面起着重要作用,但在AD中,它失去了正常的功能,并在阿尔茨海默病描述的缠结中聚集在一起。和淀粉样斑块一样,大脑用来清除多余蛋白质沉积的正常机制无法有效清除神经原纤维缠结。事实上,即使在受影响的神经元死亡后,在其内部发现的缠结仍会提醒我们原来的神经元。
随着疾病的进展,淀粉样蛋白斑块和神经纤维纤维缠结在大脑中越来越积聚。因此,这些异常结构的外观与广告症状的严重程度相关。与此同时,这些结构在疾病发展中发挥的作用仍然不清楚。例如,研究人员仍然不确定,如果淀粉样蛋白斑块本身对神经元损害,或者它们代表大脑的努力,以防止有毒Aβ肽以保护神经元免受其有害作用。有关神经纤维炎缠结的问题。他们的外表似乎是对神经元功能的破坏性,它们在大脑中的扩散与神经退化和症状的关系甚至比淀粉样蛋白斑块的增殖更密切.尽管如此,他们对广告进展的具体贡献仍然不确定。
原因和治疗
因此,仍有许多问题仍然围绕着广告的疾病过程。同样,不确定性环绕着为什么疾病影响了一些人,而不是其他人。在一小部分AD病例中,该疾病可以与少数鉴定的基因中的突变链接,其蛋白质产品参与上述Aβ肽的产生。但对于大多数患者而言,疾病没有明确的遗传或环境原因。
但是,有一些已知的风险因素。例如,称为基因的变体载脂蛋白E., 或者舆传那已知将广告的风险提高10至20次。舆传为血液中涉及胆固醇和其他脂质涉及的蛋白质编码,但尚不清楚为什么它可能涉及广告风险。然而,高脂质和胆固醇水平,也已被确定为可能的危险因素对于疾病。
有许多其他潜在的风险因素,就像吸烟,重复头部伤,心血管健康差和糖尿病.然而,研究人员仍然不确定这些因素是如何增加患AD的几率的。到目前为止,最大的风险因素仍然是我们无法避免的:老年。
因此,AD的病因仍然有些模糊,这也许使我们的治疗同样不令人满意不足为奇。这种疾病最常见的治疗方法包括使用提高神经递质水平的药物乙酰胆碱在大脑中。乙酰胆碱被认为在学习和记忆中扮演着重要的角色Nucleus Basalis.)在ad期间大量减少,可能导致记忆丧失。
称为乙酰胆碱酯酶抑制剂(ACHEIS)的药物抑制了酶的活性乙酰胆碱酯酶,其正常功能是从Synapse中除去乙酰胆碱 - 实际上降低神经递质可以在该突触处具有的效果。通过抑制乙酰胆碱酯酶活性,Acheis导致乙酰胆碱水平增加。在此过程中,这些药物可以导致记忆力的适度改善。然而,由于效果是适度的,因此,acheis在疾病的后期阶段通常不是很有用。实际上,在不到10%的患者服用药物的患者中,清楚地改善了认知症状.此外,乙酰胆碱酯酶抑制剂只能治疗ad的症状,它们对阻止疾病的发展没有任何作用。
有少数其他治疗方法,还有许多其他探索,但此时我们没有任何阻止神经变性的方法,使广告的症状下来。因此,我们在治疗疾病的能力方面保持有限。希望持续的神经科学研究允许我们开发更好的方法来解决广告大脑中发生的病理变化。
参考文献(除了上面的链接文本):
阿尔茨海默氏症(Alzheimer A, Stelzmann RA, Schnitzlein HN, Murtagh FR): 1907年阿尔茨海默氏症论文“Uber eine eigenartige Erkankung der Hirnrinde”的英译。阿娜特。1995;8(6):429 - 31所示。
Cipriani G,Dolciotti C,Picchi L,Bonuccelli U. Alzheimer及其疾病:简要历史。神经罗斯SCI。2011年4月32日(2):275-9。DOI:10.1007 / S10072-010-0454-7。
小Sanes, TM Jessell。老化的大脑。在:坎德尔ER,施瓦茨JH,杰塞尔TM,编。《神经科学原理》,第5版。纽约:麦格劳-希尔出版社。